人表皮生长因子受体2(HER2)突变型非小细胞肺癌(NSCLC)患者预后不良。德曲妥珠单抗(T-DXd)是首个获批用于治疗HER2突变型转移性NSCLC患者的靶向治疗药物,但针对HER2非19/20外显子突变患者的证据较为稀缺。本文报告了 4 例携带HER2非19/20外显子突变的转移性NSCLC患者接受德曲妥珠单抗治疗的治疗信息和结局。4 例患者均为转移性肺腺癌,且对德曲妥珠单抗治疗达到部分缓解。1 例 57 岁女性患者携带HER2 17外显子V659E突变,接受德曲妥珠单抗作为后线治疗。治疗仍在进行中,无进展生存期(PFS)已达 13 个月。3 例患者接受德曲妥珠单抗一线治疗。1 例携带HER2 3外显子T126A突变的患者在治疗 16 个月后出现疾病进展。另外 2 例患者(1 例携带HER2 21外显子H878Y突变,1 例携带HER2 17外显子V659E突变)仍在继续接受德曲妥珠单抗治疗,两者的PFS均超过 6 个月。这4例患者均未发生间质性肺病或 ≥3 级不良事件。德曲妥珠单抗在携带HER2非19/20外显子突变的转移性NSCLC患者中具有可观的潜力,值得在大样本研究中进一步验证。
背 景
肺癌是全球最常见的癌症,也是癌症死亡的主要原因,2022 年全球新发病例 248 万例,死亡病例 182 万例。大多数肺癌患者(85%)患有非小细胞肺癌(NSCLC)。人表皮生长因子受体2(HER2)突变存在于约 2% 的NSCLC病例中,且与不良预后相关。HER2突变的主要位置是20外显子和19外显子,而HER2非19/20外显子突变仅占HER2突变型NSCLC病例的约 20%。HER2突变型转移性NSCLC的首选一线治疗方案参考无驱动癌基因的转移性NSCLC(含铂化疗±免疫治疗)。疾病进展后,可选择单药化疗或免疫治疗。越来越多的生物标志物研究旨在预测治疗疗效并辅助决策,尤其是在免疫治疗时代。然而,这些治疗对HER2突变型晚期NSCLC患者的获益有限,反映出该人群对有效治疗的未满足需求。
尽管过去几十年抗HER2药物取得了巨大发展,但其在HER2突变型NSCLC中的疗效并不理想。直至 2022 年 8 月,抗HER2抗体偶联药物德曲妥珠单抗(T-DXd)基于其前所未有的疗效和可控的安全性特征,成为首个获美国食品药品监督管理局批准用于治疗携带HER2突变的转移性NSCLC患者的靶向治疗药物。DESTINY-Lung02研究的最终分析显示,在获批剂量(5.4 mg/kg,每 3 周一次)的后线德曲妥珠单抗治疗中,客观缓解率为 50.0%,中位无进展生存期(PFS)为 10.0 个月,中位总生存期为 19.0 个月。近期,该适应症也于 2024 年 10 月获得中国国家药品监督管理局批准。2025 年中国临床肿瘤学会指南已推荐德曲妥珠单抗作为后线治疗(I级推荐)。然而,既往研究主要集中于HER2 19/20外显子突变患者,而针对HER2非19/20外显子突变患者的证据较为稀缺。本文报告了4例携带HER2非19/20外显子突变的转移性NSCLC患者接受德曲妥珠单抗治疗的治疗信息和结局(表1)。
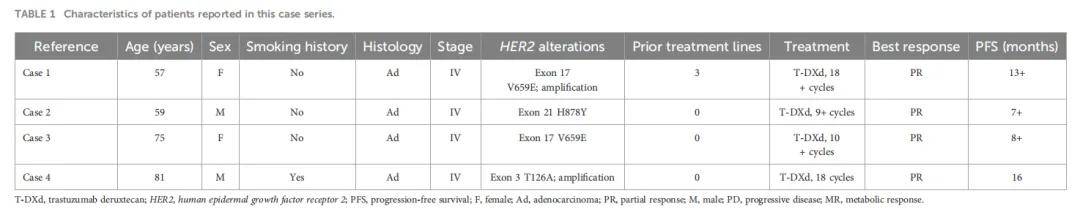
▲表1 本文病例特征
病例1
患者女,57 岁,因严重肩痛于 2020 年 5 月入院。该患者于 2019 年 7 月被诊断为右下叶肺腺癌,伴纵隔淋巴结、肝及骨转移。当时患者拒绝治疗。基因检测显示无表皮生长因子受体(EGFR)、间变性淋巴瘤激酶(ALK)或ROS原癌基因1(ROS1)突变,程序性死亡配体1(PD-L1)肿瘤比例评分(TPS)为 3%。本次入院时,影像学检查显示肿瘤进展至右肺中叶并扩散至脑。疾病分期为cT4N2M1c。患者自 2020 年 5 月起接受替雷利珠单抗(200 mg,第 1 天)联合培美曲塞(750 mg,第 1 天)、卡铂(400 mg,第1天)及贝伐珠单抗(600 mg,第 1 天)治疗,共 6 个 21 天周期,但拒绝脑及骨病变的局部放疗。2020 年 11 月,计算机断层扫描(CT)和磁共振成像(MRI)显示部分缓解(PR)。随后她接受替雷利珠单抗(200 mg,第 1 天)联合贝伐珠单抗(400 mg,第1天)维持治疗。2021 年 5 月,CT显示肺部病灶进展,肝及脑病灶稳定。她继续接受替雷利珠单抗联合贝伐珠单抗治疗,另加白蛋白结合型紫杉醇(400 mg,第1天)和卡铂(400 mg,第 1 天),共 4 个周期。2021 年 9 月,CT显示肺部病灶达到PR,肝及脑病灶稳定。随后她接受替雷利珠单抗联合贝伐珠单抗及长春瑞滨(40 mg,每周第1、3、5天)维持治疗直至 2023 年 3 月,之后接受贝伐珠单抗(300 mg,第 1 天)联合长春瑞滨(40 mg,每周第 1、3、5天)治疗。2023 年 6 月,CT显示疾病进展。长春瑞滨换为吉西他滨(1400 mg,第1、8天)联合顺铂(90 mg,第1天),同时继续贝伐珠单抗治疗。2023 年 8 月,CT和MRI显示肺及脑病灶稳定(图1A、B)。活检显示患者为微卫星稳定、PD-L1阴性,伴HER2突变(17外显子V659E)和HER2扩增。随后开始接受德曲妥珠单抗(5.4 mg/kg,每 3 周一次)单药治疗。2024 年 6 月达到PR(图1C、D),并持续至末次随访日期(2024 年 9 月)。德曲妥珠单抗治疗期间出现恶心、呕吐、肌酐升高、白细胞计数降低及肝酶升高,均为 1-2 级,经对症治疗可控制。
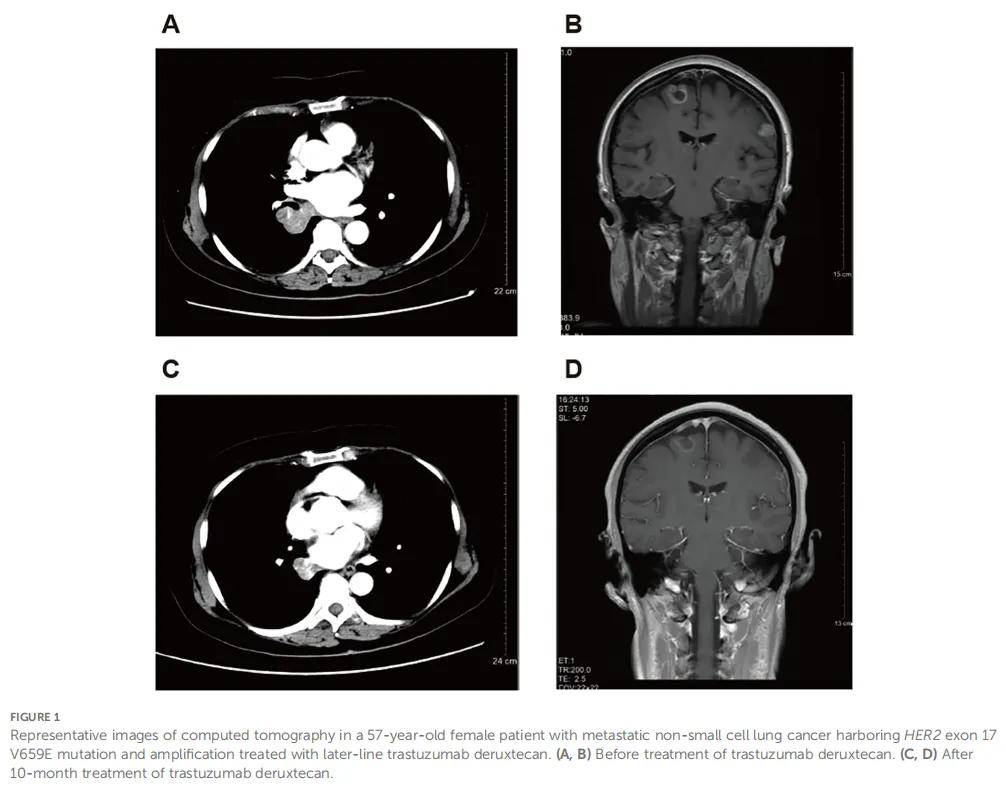
▲图1 患者代表性CT影像
病例2
患者男,59 岁,因健康体检偶然发现肿瘤标志物升高(癌胚抗原[CEA]:57.57 ng/mL;糖类抗原199[CA-199]:323.14 U/mL)于 2024 年 2 月入院。CT显示右上叶肺腺癌(21×16 mm),伴纵隔、腹膜后及腹股沟淋巴结(最大短径:14 mm)和肾上腺(21×17 mm)转移。发射型计算机断层扫描(ECT)显示骨转移。疾病分期为cT1cN2bM1c2。基因检测显示HER2(21外显子H878Y)和TP53(S241C)突变,PD-L1肿瘤比例评分(TPS)为 20%。体格检查、既往病史及实验室检查均无特殊异常。患者自 2024 年 3 月起接受德曲妥珠单抗(T-DXd)(5.0 mg/kg,每3周一次)一线治疗。2024 年 4 月,CT显示达到部分缓解(PR),并持续至末次随访日期(2024 年 10 月)。德曲妥珠单抗治疗期间未发生治疗相关不良事件。
病例3
患者女,75 岁,因咳嗽、咳痰、气喘至少持续一个月于 2023 年 11 月入院。增强CT显示大量左侧胸腔积液、左肺不张、左肺上叶炎症、左肺下叶占位性病变、左肺门淋巴结肿大、双肺多发结节、右肺下叶实性结节及左侧胸膜增厚。胸腔积液细胞学检查确诊为肺腺癌,疾病分期为TxNxM1。胸腔积液下一代测序显示HER2突变(17外显子V659E)。体格检查、既往病史及实验室检查均无特殊异常。患者自 2023 年 12 月起接受德曲妥珠单抗(T-DXd)(5.4 mg/kg,每 3 周一次)一线治疗。治疗后气喘等临床症状逐渐改善。2024 年 3 月,CT显示达到部分缓解(PR),并持续至末次随访日期(2024 年 8 月)。德曲妥珠单抗治疗期间出现恶心、呕吐、贫血、天冬氨酸转氨酶升高及直接胆红素升高,均为 1-2 级,经对症治疗可控制。
病例4
患者男,81 岁,因转移性非小细胞肺癌(NSCLC)治疗于 2023 年 3 月入院。该患者于 2020 年 6 月被诊断为左下叶低分化肺腺癌,并接受了胸腔镜辅助根治性切除术。病理分期为T2aN1M0。术后,患者于 2020 年 7 月至 2020 年 8 月接受培美曲塞(700 mg,第 1 天)联合奈达铂(100 mg,第 2 天)辅助化疗,共 2 个 21 天周期,后因无法耐受毒性而停药。2023 年 2 月,CT显示双肺转移性肿瘤病灶。患者有冠心病、重度高血压病史,吸烟史70年。本次入院时,体格检查及实验室检查显示完全性右束支传导阻滞,血红蛋白 78 g/L,东部肿瘤协作组(ECOG)体力状况评分为 3 分,无其他显著异常。CT显示双肺多发结节(最大者边界不清:49×28 mm),残余左肺炎症伴癌性淋巴管炎,多发淋巴结转移(锁骨上窝、膈脚、左心膈角、右肺门及纵隔;最大短径:23 mm),左侧胸膜增厚(图2A、B)。疾病分期为rpT4N3M1a。采用手术切除标本进行基因检测,结果显示HER2突变(3外显子T126A)及HER2扩增。患者自 2023 年 3 月起接受德曲妥珠单抗(T-DXd)(3.4 mg/kg,每3周一次)治疗,最佳疗效为部分缓解(PR)(图2C、D),ECOG体力状况评分改善(从 3 分降至 1 分)。德曲妥珠单抗单药治疗18个周期期间,出现恶心、乏力,均为 2 级。2024 年 7 月,彩色超声显示左锁骨上淋巴结转移,CT显示疾病进展(图2E、F)。随后在德曲妥珠单抗治疗基础上加用安罗替尼(10 mg,每日一次)。1 个 21 天周期治疗后,因耐受性差,德曲妥珠单抗换为培美曲塞(700 mg,第 1 天),同时继续安罗替尼治疗。
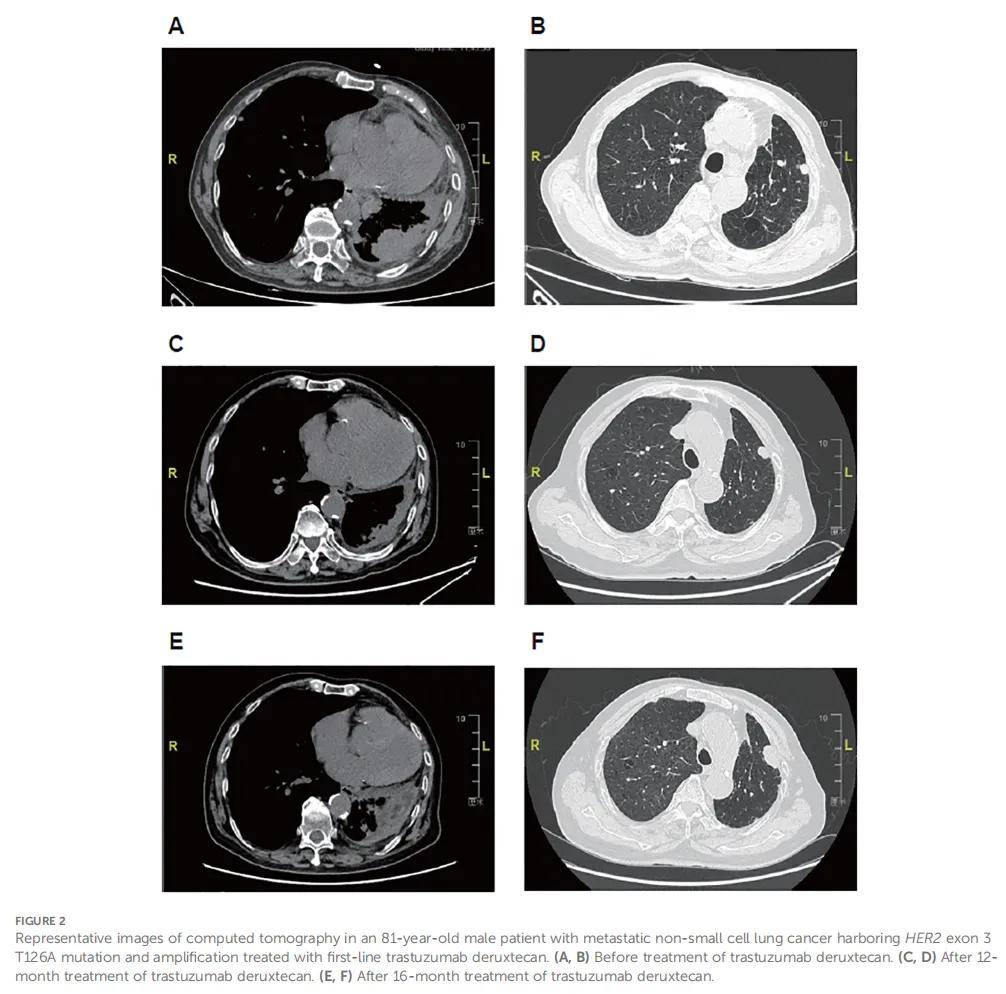
▲图2 患者代表性CT影像
讨 论
HER2突变位置的差异可能会影响对抗HER2治疗的敏感性。由于HER2非19/20外显子突变较为罕见,目前仍缺乏可靠的证据和成熟的治疗方案。尽管德曲妥珠单抗(T-DXd)已获批用于治疗HER2突变的转移性非小细胞肺癌(NSCLC),但其在HER2非19/20外显子突变患者中的疗效尚未完全明确。关键的DESTINY-Lung01和DESTINY-Lung02试验主要纳入了HER2 19/20外显子突变患者。既往发表的德曲妥珠单抗病例报告仅公布了HER2 20外显子突变NSCLC患者的个案数据。本文补充了该临床场景下的具体疗效和安全性数据,可为临床医生提供一定参考。
病例1确诊时即为晚期肺腺癌,伴多发器官转移。该患者无驱动癌基因,PD-L1肿瘤比例评分(TPS)为 3%。考虑到患者相对年轻,给予免疫治疗联合化疗及抗血管生成治疗的四药联合方案。尽管每次疾病进展后均更换化疗药物,患者仍在 3 年内经历了两次治疗失败。在化疗联合抗血管生成治疗的三线治疗期间,经活检检测到HER2突变。尽管患者携带的是罕见的17外显子V659E突变而非19/20外显子突变,仍接受了德曲妥珠单抗单药治疗,最佳疗效为部分缓解(PR)。作为后线治疗,至少13个月的无进展生存期(PFS)无疑令人鼓舞。DESTINY-Lung01和DESTINY-Lung02试验共纳入 8 例既往接受过治疗的HER2非19/20外显子突变转移性NSCLC可评估患者。其中 3 例(38%)接受德曲妥珠单抗治疗后达到PR,4 例达到病灶缩小的疾病稳定(SD),提示疾病控制良好。关于其他抗HER2治疗,既往一些研究探索了泛HER酪氨酸激酶抑制剂在该人群中的应用。Song等开展的II期试验探讨了吡咯替尼在HER2突变晚期肺腺癌患者中的疗效,70.5% 的患者接受吡咯替尼作为二线及以上治疗。该试验共纳入 10 例HER2非19/20外显子突变患者,但仅 1 例17外显子突变患者接受吡咯替尼治疗后达到PR,客观缓解率(ORR)为 10%。在Ou等的研究中,1 例HER2 17外显子突变(V659E/G660R)的转移性肺腺癌患者接受二线阿法替尼治疗后达到PR,PFS至少 18 个月。另 1 例HER2 17外显子V659E突变的转移性肺腺癌伴腹膜转移患者接受阿法替尼治疗 3 个月后,症状显著改善并达到代谢缓解。然而,1 例HER2 17外显子G660D突变的转移性肺腺癌患者接受二线阿法替尼治疗10周后出现疾病快速进展。所有这些结果提示,德曲妥珠单抗在后线治疗HER2非19/20外显子突变转移性NSCLC患者中具有潜在疗效,值得进一步验证。由于样本量较小,HER2非19/20外显子突变患者接受德曲妥珠单抗治疗的临床获益与HER2 19/20外显子突变人群是否一致或存在差异,仍需进一步研究。
本病例系列中的其他 3 例患者均在一线治疗场景下接受德曲妥珠单抗治疗,且均达到PR。值得注意的是,病例4在德曲妥珠单抗治疗直至疾病进展前的PFS达到 16 个月。尽管病例2和病例3的随访时间较短,无法反映长期生存获益,但二者在接受德曲妥珠单抗治疗 1-3 个月后均出现快速缓解。国际多中心随机对照III期DESTINY-Lung04试验(NCT05048797)正在进行中,旨在证实德曲妥珠单抗作为HER2 19/20外显子突变晚期NSCLC患者一线治疗的作用。本文结果初步显示,德曲妥珠单抗一线治疗HER2非19/20外显子突变患者具有潜在价值,值得进一步研究。在Ou等的研究中,1 例HER2 17外显子V659E突变的转移性肺腺癌伴骨转移患者接受阿法替尼一线治疗 1 个月后快速缓解,但随访时间不足。目前尚无更多关于阿法替尼或其他抗HER2治疗用于HER2非19/20外显子突变转移性NSCLC患者的一线数据公布。
这 4 例患者的不良事件谱均可接受。未发生间质性肺病(ILD)或≥3级不良事件。随着德曲妥珠单抗的广泛应用,不良事件的监测与预防将更加规范化,临床实践中对其毒性风险的担忧也会减少。对于 2 例 ≥75 岁的老年患者,仅观察到轻度胃肠道反应、贫血、乏力及肝胆毒性。81 岁患者接受德曲妥珠单抗治疗后,ECOG体力状况评分显著改善,提示其在可能无法耐受化疗的老年患者中具有可行性。
本病例系列存在一些局限性。首先,样本量确实过小,无法得出令人信服的结论。其次,4 例患者中有 2 例随访时间较短。迫切需要大规模前瞻性、长期随访的证据来验证我们的发现。总之,本病例系列初步显示,德曲妥珠单抗在携带HER2非19/20外显子突变的转移性NSCLC患者中具有潜在疗效和可接受的安全性。这些发现值得进一步大样本验证。
参考文献:
Meng Y, Du Y, Liu X, Huang J, Chen H and He C (2025) Trastuzumab deruxtecan for the treatment of metastatic non-small cell lung cancer harboring HER2 non-exon 19/20 mutations: four case reports. Front. Immunol. 16:1631768. doi: 10.3389/fimmu.2025.1631768





