日前,国务院总理李强签署国务院令,公布《生物医学新技术临床研究和临床转化应用管理条例》(以下简称《条例》),自2026年5月1日起施行。
作为率先实践介入微创与细胞联合治疗的先行者,中国中西医结合学会介入医学专业委员会副主委,中国中医药信息学会中西医结合介入分会执行会长兼秘书长,车能雨教授从《条例》出台的背景,意义,内容,临床转化,法治力量,未来展望等方面进行了解读和展望。作为深耕多年介入医学和细胞治疗临床工作的医生,车能雨教授深感这一《条例》的出台恰逢其时,为生物医学新技术临床研究与应用提供了明确法律框架,既促进创新,又保障安全。
一,法律出台背景
近年来,生物医学领域创新活跃,以细胞治疗,基因编辑为代表的生物医学新技术层出不穷,为众多难治性疾病带来希望。
以车能雨教授团队开展的CAR-T细胞免疫治疗为例,通过微创介入联合细胞治疗,靶向治疗等,让晚期肺癌患者肿瘤缩小约90%,为后续根治创造了宝贵时间窗口。
然而,新技术在带来希望的同时,也伴随着风险和伦理挑战。如何在促进创新与保障安全之间取得平衡,成为立法者面临的重要课题。
《条例》的颁布实施,正好填补了我国在生物医学新技术领域的法律空白,为临床研究和转化应用提供了制度保障。
二,重大意义
为医疗创新应用提供制度保障
车能雨教授认为,《条例》的出台将对整个行业产生深远影响。
促进规范发展。《条例》确立了生物医学新技术从实验室研究到临床转化应用的全过程管理制度,使创新活动有法可依,有章可循。
车能雨教授表示:“以前我们在开展细胞治疗时,常常面临标准不统一,监管不明确的困境。《条例》实施后,研究人员和患者都将拥有更明确的法律保障。”
保障医疗质量安全。《条例》要求国务院卫生健康部门对已备案的临床研究进行评估,发现风险及时纠正直至叫停。
同时,规定临床研究机构应当采取措施,预防控制和处置研究实施中的风险。
推动合规创新。《条例》不仅注重规范,也鼓励创新。
国家采取措施促进生物医学新技术创新发展,鼓励和支持生物医学新技术临床研究和临床转化应用。
三,核心内容
《条例》共7章58条,涵盖了总则,临床研究备案,临床研究实施,临床转化应用等主要内容。
从临床医生的视角看,以下几方面的规定对我们工作影响最为直接:
临床研究机构门槛提高
《条例》明确规定,实施生物医学新技术临床研究的机构必须是三级甲等医疗机构,且需具备符合要求的临床研究学术委员会和伦理委员会。
这一规定确保了生物医学新技术临床研究在设施,设备,专业技术人员和管理制度方面的高标准,为受试者安全提供了基础保障。
双重审查制度确立
《条例》要求临床研究机构必须通过学术审查和伦理审查,方可开展临床研究。
这意味着任何生物医学新技术临床研究不仅要有科学价值,还必须符合伦理原则,维护人的尊严和健康,这体现了立法对人民健康高度负责的态度。
备案管理要求明确
根据《条例》,临床研究机构应在通过学术审查和伦理审查之日起5个工作日内向国务院卫生健康部门备案。
备案制度既不像过去那样放任不管,也不过于严苛阻碍创新,体现了“放管服”改革精神,有利于促进生物医学新技术健康发展。
受试者权益保障
《条例》在受试者权益保护方面作出了详尽规定,体现出浓厚的以人为本精神。
知情同意权的保障是核心内容之一。《条例》要求临床研究机构必须以受试者或其监护人容易理解的方式告知研究目的,方案及可能风险。
在车能雨团队的临床实践中,早已发现充分知情同意不仅是法律要求,也是建立医患信任的重要基础。
禁止收费是另一重要保障。《条例》明确规定临床研究发起机构和实施机构不得向受试者收取与生物医学新技术临床研究有关的费用。
这一规定避免了经济利益驱动可能带来的伦理风险,确保研究纯属科学探索而非商业行为。
损害赔偿机制也为受试者提供了重要保障。《条例》规定临床研究造成受试者健康损害的,临床研究机构应当及时予以治疗。
临床转化应用规范
《条例》对生物医学新技术的临床转化应用设置了明确路径。临床研究证明安全,有效且符合伦理原则的生物医学新技术,经国务院卫生健康部门批准,可以转化应用于临床。
这一规定改变了以往生物医学新技术临床应用缺乏明确监管标准的状况,为安全有效的技术创新转化为临床实践提供了合法通道。
对广大患者而言,这意味着未来能够更快,更安全地享受到生物医学新技术带来的健康福祉。
四,对医疗行业的影响
《条例》的实施将对医疗行业产生深远影响,三级甲等医疗机构将在生物医学新技术创新中承担更重要责任,也给三甲医院发展带来机遇和挑战。
从医院角度来看,《条例》的出台为医院开展生物医学新技术临床研究和转化应用提供了明确的指导和规范。医院在进行相关研究和应用时,必须严格遵循《条例》要求,坚持以人民健康为中心,确保新技术具有科学依据,加强全过程安全管理。例如,在临床研究项目的审批环节,医院需要更加严格地审核项目负责人的资格,根据《条例》规定,项目负责人应当具备执业医师资格和高级职称,具有良好的职业道德,科学研究信誉和临床技术水平等,如果项目负责人有生物治疗高级职称资质或相应培训合格证书,医院应该优先审批通过并优先开展项目研究,这就相当于项目负责人有证驾驶生物治疗这辆新车,从法理上规避了无证驾驶的风险。这将促使医院进一步完善内部审核机制,提高研究项目的质量和安全性。
对医院管理者而言,需要建立健全临床研究学术委员会和伦理委员会,可建立门诊,病房,实验室等完整的生物治疗闭环,完善相关管理制度,为合规开展生物医学新技术临床研究创造条件。
同时,未来可能进一步规范临床行为,要求从事生物治疗(包含细胞治疗和非细胞治疗)医生需要进一步取得生物医学临床相关资质,如生物治疗职称证书或者培训合格证书,提高生物治疗水平,还必须适应在新的法律框架内开展工作,加强伦理意识和法律意识培训学习,在创新同时保障患者安全。对于医生而言,《条例》既是一种约束,更是一种保护。一方面,医生在开展生物医学新技术临床研究和临床转化应用时,需要严格遵守法律,行政法规和国家有关规定,不得危害人体健康,不得违反伦理原则。这要求医生在实践中要保持高度的责任感和职业道德,确保每一项新技术的应用都符合患者的利益和社会的公共利益。另一方面,《条例》也为医生提供了一个合法合规的操作框架,当医生按照《条例》要求开展工作时,其合法权益将得到保障。同时,《条例》鼓励和支持生物医学新技术临床研究和临床转化应用,这也为医生提供了更广阔的创新和发展空间,有助于医生提升自身的专业水平和技术能力。
从事生物治疗(包含细胞治疗和非细胞治疗)医生需要进一步取得生物医学临床相关资质,如生物治疗职称证书或者培训合格证书,建议卫生行政部门加快生物治疗培训考核力度,或者加快成立生物治疗或细胞基因治疗专业学术组织,协助培训生物治疗或细胞基因治疗专业从业者,适应生物技术临床应用需求。同时呼吁高等院校科研院所加快设立生物医学或细胞基因治疗临床专业,迎接社会对生物技术的蓬勃发展。
五,未来展望
几年前,车能雨就提出医学发展“内科外科化,外科微创化,微创介入化,介入中西化”的趋势。如今,他进一步指出:“生物医学(细胞与基因治疗)技术的突破性进展,尤其是CAR-T技术在血液肿瘤中的特异性效果,已经远超传统药物甚至部分手术的局限。它不再局限于某一科室的辅助手段,而是可能成为继内科,外科,介入科之后的第四大学科。”
《条例》的出台,从政策层面为这一学科诞生提供了可能。他解释:“生物治疗涉及免疫学,细胞学,基因工程,临床医学等多学科交叉,需要进一步的诊疗规范,人才培养体系和医保支付支持。《条例》出台为这一学科体系化发展‘铺路’”。
《条例》将于2026年5月1日起施行,距今有半年多的准备期。这段时间对医疗机构至关重要,我们应当认真学习《条例》内容,提前做好各项准备。
多年来,车能雨教授团队通过“微创介入+细胞治疗+靶向治疗”组合方案,让一些恶性肿瘤患者肿瘤缩小,临床症状改善,为患者达到NED状态创造了宝贵机会。
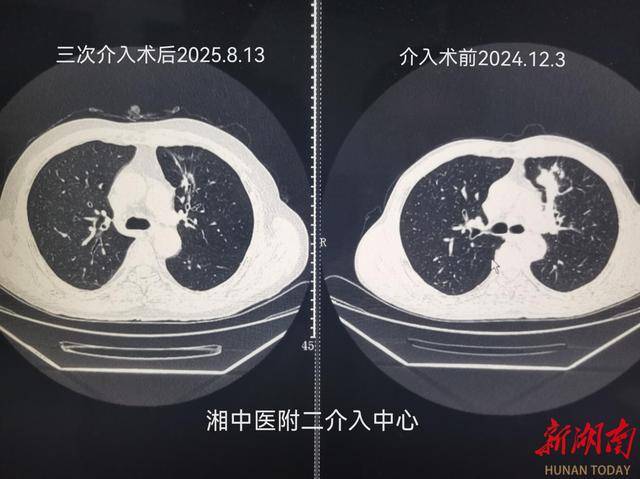
病友男,55岁,肺癌,三次介入微创+CAR-T 细胞治疗后,肺癌缩小90%左右,脊柱多发转移灶失去活性,达到NED状态。
“《条例》实施后,像这样成功的案例将会更多。”车能雨教授说,新技术,新方法将在法治的轨道上更快更好地造福患者。
CAR-M疗法作为新兴的生物医学技术,与CAR-T一样面临着临床转化的挑战。该疗法通过改造巨噬细胞使其能够“吃掉”癌细胞,同时改善肿瘤微环境,为肿瘤治疗提供了新思路。
《条例》的出台将为这些新技术提供清晰的研发路径和审批流程,加速其从实验室走向临床。
随着2026年5月1日《条例》正式施行的临近,中国生物医学新技术领域正迎来创新与监管协同发展的新阶段。
车能雨教授预计,随着《条例》的实施,我国在生物医学新技术领域的研究将更加规范有序,创新活力将进一步释放。正如《条例》所倡导的,安全与创新并重,才是生物医学新技术发展的正确道路。
三甲医院有生物治疗资质临床医生将在《条例》框架下,积极稳妥地推进生物医学新技术的临床研究和应用,让更多患者从医学创新中受益。
总之,《生物医学新技术临床研究和临床转化应用管理条例》的颁布实施,对于医院和医生来说是一次重要的机遇和挑战。我们将以《条例》为指导,不断规范生物医学新技术的临床研究和转化应用,为促进医学科学技术进步和创新,保障人民群众的健康权益做出更大的贡献。
专家简介:车能雨教授,介入医学专家,细胞和基因临床应用资深专家,第一批“全国卫生健康技术推广应用传承人”,中国中西医结合学会介入医学专业委员会副主任委员,中国中医药信息学会中西医结合介入分会执行会长兼秘书长,中国医药教育协会肿瘤内照射专业委员会副主任委员,亚洲冷冻治疗学会常委,湖南省医院协会血管病专业委员会委员,湖南省妇幼保健协会妇产介入专委会副主任委员,《中国介入影像与治疗学》杂志编委。
来源:大众卫生报·客户端





