二十年前研究者就发现,自闭症与肠道菌群异常间存在因果关联。自闭症儿童的肠道菌群发生了明显改变,将自自闭症儿童的肠道菌群移植给无菌小鼠就足以诱发小鼠的自闭症样行为和认知表现。
食与心研究室更早在22年前就发现了肠道微生物在自闭症中的关键作用。20年来通过 补充益生菌+饮食调整 改善肠道微生物,恢复菌-肠-脑轴功能已经帮助不少自闭症儿童恢复正常发育,让他/她们跟同龄孩子一样正常上学。同时也对很多已经进入青壮年的自闭症患者予以积极的 微生物+饮食 干预,显著降低了他们的易亢奋和攻击性倾向。
食与心在公众号创立之后持续介绍过该领域的研究发现和最新进展,并且不断更新。对于关心自闭症孩子及其家人的人来说,肠道微生物研究领域的每一次进展都非常振奋人心。
但对于很多相信自闭症是基因问题/命运问题/或者其他问题的人来说,反而这个领域每一次对于肠道微生物作用的质疑似乎更让他/她们兴奋、更加认为自己坚持的观点是正确的。
2021年国际高分期刊《cell》杂志的一项研究在学术界和自闭症机构以及众多家长中引起过白热化的讨论。

那个研究团队在对247名2-17岁自闭症儿童进行了粪便宏基因组学研究后得出结论:自闭症与肠道微生物之间的直接关联可以忽略不计,自闭症相关的菌群差异主要由自闭症儿童的饮食偏好造成。【1】
然而之后至今的研究并没有重复同样或类似的结果,相反,肠道微生物影响自闭症的机制却在不断被揭示。
本期食与心本期食与心结合今年(2025年)的三项研究来介绍肠道微生物影响自闭症的途径,以及这些途径给我们带来了什么启示。
——1. 色氨酸相关肠道代谢物与自闭症症状
2025年4月《Nature Communications》的一项研究结合粪便代谢组学检测、功能性磁共振成像 (fMRI)和行为评估分析了神经典型儿童(正常发育)和自闭症儿童的差异,参与者年龄范围在8-17岁。【2】
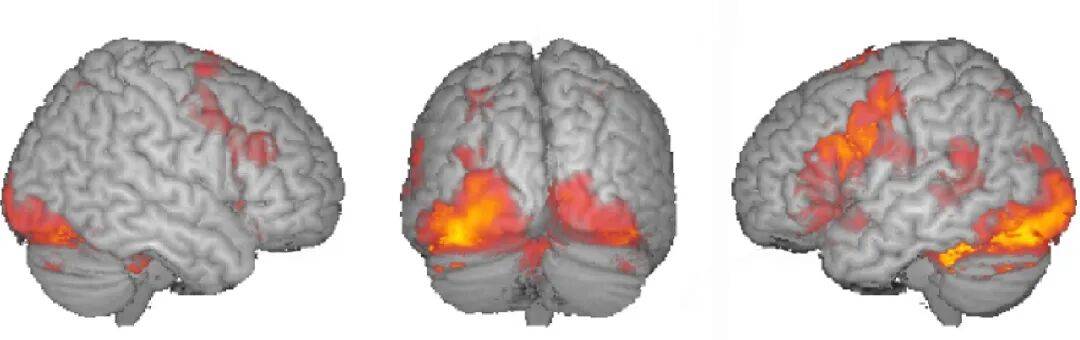
结果发现,与神经典型组相比,ASD组在以下方面显示出显着更高的值:体重指数 (BMI)、产前抗生素使用、胃肠道症状、感觉敏感性、注意力缺陷/多动障碍 (ADHD) 症状、厌恶敏感性、厌恶倾向和社交困难。此外,ASD 组在满量程智商 (FSIQ) 和睡眠质量方面的得分显著较低。
感觉敏感性和厌恶敏感性在听觉居然也会过敏!和为什么有的孩子/大人会挑食?有介绍,比如自闭症的孩子可能对特定声音异常敏感和恐惧,对某些食物的味道异常厌恶。胃肠道症状在为什么自闭症干预需要长期过程也进行了介绍。智力发育、排便和睡眠方面家长们往往感触更深。
食与心研究室也发现,自闭症的孩子随年龄和认知能力渐升,继而转为ADHD症状;随着年龄增加,还可能出现秽语抽动症状。(调整菌群能改善抽动症吗)
这项研究中,粪便代谢组的分析显示:与神经典型儿童相比,自闭症儿童粪便中特定色氨酸相关代谢物(特别是犬尿酸盐)水平显著降低。
吲哚代谢物、大脑活动(岛叶亚区域、dmPFC/aMCC、IFGop 和 S1)和症状(自闭症严重程度 [ADI-R RSI] 和述情障碍)之间存在多种相关性。较高水平的色氨酸酚与感觉敏感性(前庭/本体感觉、社会性和非社会性)显著相关。较高水平的邻氨基苯甲酸盐与较高的睡眠质量显著相关。
中岛叶和中扣带回的活性显著介导微生物色氨酸代谢物(吲哚乳酸和色氨酸甜菜碱)与 ASD 严重程度和厌恶敏感性之间的关系。这一点特别值得注意,因为:1)厌恶处理与内感受处理密切相关,受肠道代谢物的影响明显; 2)自闭症谱系障碍儿童在厌恶处理方面通常存在异常; 3) 中岛叶是内感受、情绪和化学感觉处理的中心,尤其以自闭症谱系障碍中表现出非典型活动和连接而闻名。
色氨酸是人体必需氨基酸之一,来源于饮食。它不仅参与蛋白质合成,还可作为多条代谢通路的前体,生成多种重要的代谢物,涉及 神经递质、免疫、能量代谢、肠-脑轴 等多个方面。
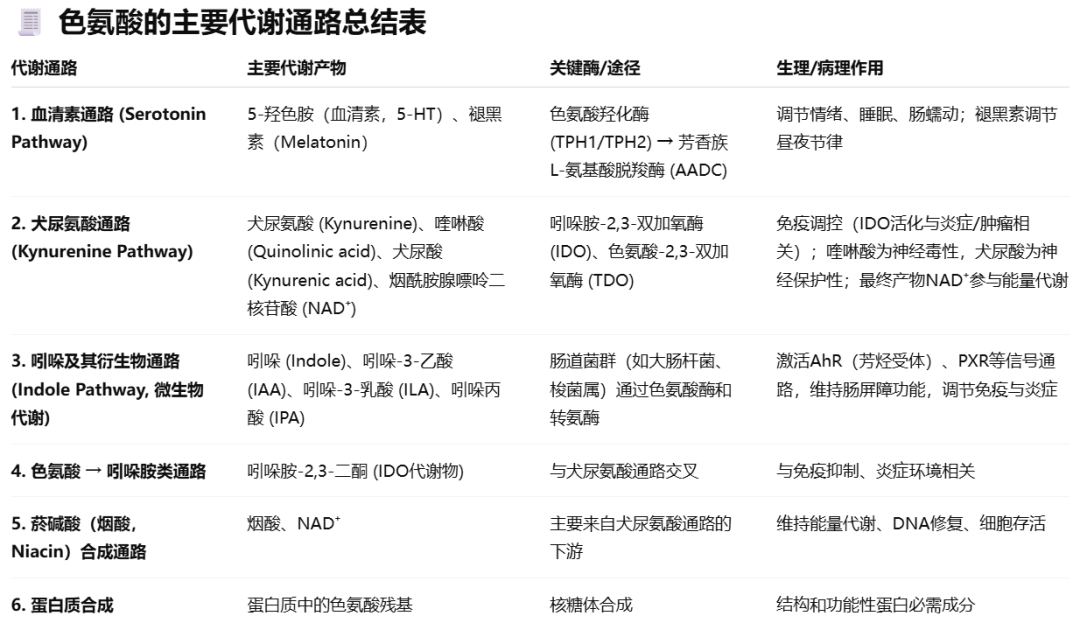
色氨酸在人体主要代谢方向是前两条:
① 犬尿氨酸通路(>90%,偏向免疫与能量代谢)
② 血清素(5-HT)通路(约1–2%,影响神经/情绪/睡眠)
微生物通过产生 吲哚类代谢物 调节肠屏障和免疫,目前已被确认与自闭症、抑郁症、炎症性肠病等相关。
这项研究发现与2021年研究完全相反,自闭症儿童和神经典型儿童的饮食并没有显著差异,自闭症儿童更可能有产前(母体)抗生素使用。
自闭症相关的肠道微生物是驱动自闭症的关键因素,这种异常的肠道微生物可能通过影响色氨酸代谢物(比如吲哚)改变了大脑厌恶敏感性,进而引发了厌恶行为和各种自闭症症状,比如特殊的食物选择。
而改变色氨酸肠道代谢的方法很多,比如补充瑞士乳杆菌NS8,增加膳食纤维和果胶等摄入。(色氨酸真的伤肾促癌吗?)
——2. 谷氨酸/GABA系统平衡与自闭症
BTBR 小鼠模型(BTBR T+ Itpr3tf/J,简称 BTBR)是一种常用的自闭症谱系障碍研究模型小鼠。它们源自近交系小鼠,因其在社会行为、沟通方式以及重复刻板行为等方面表现出典型的 类自闭症表型,而被广泛用于神经科学和精神疾病研究。
BTBR 小鼠模型携带有ASD相关基因,伴有菌群失调和全身炎症,可能存在肠-免疫-大脑轴功能异常。

2025年7月《 Nature Communications》的一项研究使用了无菌 BTBR 小鼠模型。研究者通过胚胎移植和在GF隔离器中饲养,产生了一系列无菌BTBR小鼠(GF BTBR)。【3】
检测发现:无菌状态下,缺乏肠道微生物群的雄性BTBR 小鼠不仅ASD相关行为减少,炎症性脑驻留 T 细胞的数量也显著降低。这一发现提示:肠道微生物群可能决定了脑驻留T细胞的功能活性和驻留表型,在GF BTBR小鼠中观察到的行为变化可能源于T细胞介导的神经炎症的减弱。
脑驻留T 细胞(brain-resident T cells)是指在中枢神经系统内长期存在并具有免疫功能的 T 细胞群体,主要在脑实质、脑膜和脉络丛中被发现。它们不同于外周循环 T 细胞,表现出“组织驻留”特征(如 CD69、CD103 高表达),参与神经炎症、感染防御以及神经退行性疾病的病程调控。
脑驻留T细胞的主要有五种类型,如下表所示:

以往研究发现,CD4 T 细胞是小胶质细胞的正常成熟以及海马神经发生所必需的,CD4 T细胞可调节神经典型B6小鼠的重复和焦虑样行为。
研究者对于有菌群(SPF)的BTBR 小鼠通过施用单克隆抗体耗竭CD4 T细胞,发现CD4 T 细胞耗竭可减轻神经炎症和 ASD 行为,进一步表明存在肠-免疫-脑轴。
结合无菌BTBR小鼠的表现,研究者推测是某些肠道微生物的变化改变了脑驻留CD4 T细胞,进而引发了自闭症表现。
研究者接着通过抗生素处理实验和粪菌移植实验再次验证了肠道菌群与自闭症行为之间的关联。粪便代谢组学分析还确定了ASD 相关代谢调节因子,特别是与谷氨酸/GABA 比率和 3-羟基戊二酸相关的调节因子。
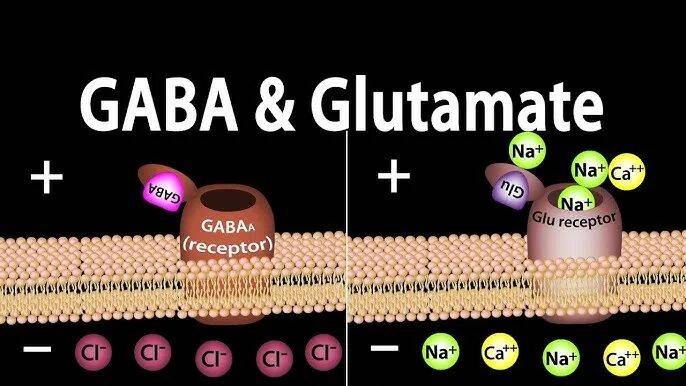
临床研究也发现,ASD 患者的粪便中存在较高的谷氨酸和较低的 GABA 浓度,表明 ASD 存在兴奋性/抑制性失衡。3-羟基戊二酸是一种神经毒素,在 ASD 微生物群中也高度富集。这种代谢物与许多行为和认知缺陷有关,部分原因是因为能诱导谷氨酸能和 GABA 能失衡 。
微生物分析揭示诱发BTBR小鼠谷氨酸/GABA 失衡的原因可能是一种乳酸杆菌L. murinus 。单菌喂养实验发现,BTBR 小鼠背景下补充L. murinus 足以驱动 ASD 相关行为和神经炎症。
3周龄时通过同笼饲养将来自神经典型B6小鼠的肠道菌群移植给无菌BTBR小鼠,8周龄时能检测到自闭症行为显著减少。健康的肠道微生物群不仅可以保护BTBR小鼠免受ASD相关行为的影响,也通过增加脑驻留Treg数量减少了CD4 T 细胞分泌的IFN-γ,同时改变了小胶质细胞类型,让小胶质细胞分泌更多抗炎症细胞因子(IL-10),更少促炎症细胞因子(IL-6、IL-1β和TNF-α)。这些结果提示,无论遗传背景如何,肠道微生物群都可能决定自闭症行为和神经免疫表型。
结合代谢组和菌群的分析发现,健康的肠道微生物群可以改变代谢物库,以减轻兴奋性/抑制性代谢失衡并抑制神经炎症,从而保护 BTBR 小鼠免受 ASD 相关行为的影响。
使用计算机代谢物预测模型,研究者将能够高 GABA 产生和谷氨酸摄取的罗伊氏乳杆菌菌株确认为益生菌候选者,并通过活菌补充实验检测了这种菌株的效果。结果发现,补充这种罗伊氏乳杆菌菌株通过改变代谢物库(降低谷氨酸/GABA 比率)和调节神经炎症(增加Treg数量,减少CD4 T 细胞和CD8 T细胞分泌的IFN-γ)来改善 ASD 相关行为。
小结下这项研究中的几项关键发现:
- 肠道微生物群通过调节脑驻留 T 细胞和小胶质细胞群来调节 ASD 表型和神经炎症;
- CD4 T 细胞驱动 ASD 发病机制;
- L. murinus 能够通过上调谷氨酸/GABA 比率和神经毒性 3-羟基戊二酸来诱导 ASD 样行为;
- 源自B6小鼠或益生菌菌株罗伊氏乳杆菌IMB015的有益肠道菌群,通过减少致病代谢物和抑制神经炎症来缓解ASD表型。
这些发现表明,肠道微生物群及其与宿主免疫的相互作用可以取代ASD背后的遗传易感性。
这与食与心研究室的干预研究可相互印证,补充瑞士乳杆菌NS8+发酵乳杆菌NS9不仅能改善自闭症儿童的胃肠道症状和行为认知异常,还能恢复谷氨酸/GABA平衡。
对于遗传抑郁模型大鼠的研究也发现了NS8改善肠道谷氨酸/GABA平衡的能力。NS8促进Treg分化的能力也在多项行为生物学实验中得到验证。
需要注意的是:虽然本研究中的罗伊氏乳杆菌菌株发挥了抗自闭症作用,之前也有相似研究罗伊氏乳杆菌干预纠正自闭症小鼠社交缺陷。但也有研究发现罗伊氏能代谢色氨酸产生吲哚,进而可能胰腺癌发展乳酸杆菌真的促癌吗?。食与心在遗传抑郁大鼠研究中也发现,罗伊氏乳杆菌的影响可能与NS8相反。食与心实验室在筛选制作酸奶的独特微生物菌株时发现,罗伊氏乳杆菌发酵牛奶时还可能产生酒精,因此在自行制作益心菌的时候淘汰了罗伊氏乳杆菌。
——3. 苯甲酸钠与星形胶质细胞
2025年8月《Molecular Psychiatry》的一项研究通过自闭症队列的分析确认,乳酸杆菌定植可能通过调节特定的微生物代谢途径来改善 ASD 患者胃肠道和神经系统症状的严重程度。【4】
接下来,研究者通过母体免疫激活 (MIA)诱发的ASD小鼠模型来验证这种假设。
结果发现,补充植物乳杆菌或其衍生的苯甲酸钠(NaB)可以减轻肠道菌群失调,减轻自闭症小鼠的社会行为缺陷,谷氨酸-谷氨酰胺水平和神经元活动。 NaB 可能通过增加增强子区域的 H3K27 苯甲酰化结合来增强星形胶质细胞中的 Cxcl16 基因表达,进而改善了神经元和星形胶质细胞之间的谷氨酸代谢。
食与心温馨总结:虽然很多人坚定笃信基因在自闭症中的作用,但2025年的最新研究再一次确认了肠道微生物在自闭症中的因果作用。
肠道中的某些微生物比如特定乳酸杆菌可能通过调节色氨酸代谢,影响犬尿酸、吲哚等关键产物来改变大脑,从而影响自闭症相关的行为和厌恶敏感性。
特定乳酸杆菌可通过影响谷氨酸/GABA平衡,来影响脑驻留T细胞的类型(CD4 T 细胞 VS Treg),进而影响小胶质细胞分化,从而影响自闭症相关行为和神经炎症。即使是对于遗传易感性的自闭症小鼠,乳酸杆菌的作用依然不受影响。
植物乳杆菌也有可通过苯甲酸钠途径改变星形胶质细胞基因表达,进而影响谷氨酸代谢,改善自闭症相关行为和神经元活动。
这些发现表明,易感基因只是决定了自闭症的可能风险,是否真的罹患自闭症得看肠道菌群。小鼠的实验表明,没有携带易感基因的品系仅仅通过粪便的转移也能让其表现出自闭症样行为,说明自闭症相关菌群也足以诱发自闭症;而即便携带易感基因,健康的肠道菌群也能减少自闭症的行为和生理异常,让个体恢复正常。那些能参与色氨酸代谢、谷氨酸/GABA系统的微生物在这个过程中发挥重要作用。
需要强调的是:虽然同为乳酸杆菌属,不同菌株的影响差异巨大。如果想要通过补充乳酸杆菌改善自闭症,一定要选择那些有益的菌株,比如调节蛋白质代谢的瑞士乳杆菌NS8,诱导免疫系统正常运行的发酵乳杆菌NS9,又能调节脂代谢,又能促进短链脂肪酸生成的植物乳杆菌NS5等优秀菌株,而不是火上浇油的L. murinus乳杆菌或者有时会翻脸的罗伊氏乳杆菌。
写到这里,不禁有很多人会问,这些菌吃了不会产生依赖吗?需要一直吃下去吗?甚至有些医生也说,外来微生物长期使用会改变自己原本的肠道微生态,有害……
事实上,正常的人也许不需要补充任何类型的微生物,但是对于目前医学上都宣布为不治之症的自闭症,没有比 有效微生物制剂+高膳食纤维饮食 更安全的治疗方法,而食与心实验室多年的实践成功逆转了很多自闭症患者,带他们走出了自闭症阴影。
也有人问,这些微生物能定植吗?回答这个问题之前食与心先普及一下基础知识:你养一只猫,你给它准备了很多青菜和胡萝卜,你能期待猫在你家里正常生存和繁殖吗?当然不能,因为你没有选择正确的食物。因此,除了补充有益微生物外,通过健康的饮食来给有益微生物正确的营养物,促进它们生长才是健康之本。
食与心多次强调过,食物决定微生物,微生物调控免疫系统,神经系统,内分泌系统和消化系统。这四个系统决定着人的生老病死和幸福感。牢记这个顺序和机理,那么大多数人都能远离神经系统发育障碍。
参考材料
1. https://www.cell.com/cell/fulltext/S0092-8674(21)01231-9?
2. https://www.nature.com/articles/s41467-025-58459-1
3. https://www.nature.com/articles/s41467-025-61544-0
4. https://www.nature.com/articles/s41380-025-03164-0





