早在上世纪80年代,就有学者发现:NK活性较低者,十年内的癌症发病率显著升高。随后的实验进一步印证:增强NK活性,肿瘤发生率明显下降。
多项流行病学研究证实,NK 细胞活性与癌症发生率呈负相关。2022 年发表在《Cancer Research》的一项研究显示,对 1200 名健康人群随访 5 年,NK 细胞活性处于低水平(杀伤率 <30%)的人群,癌症发病风险是高活性人群(杀伤率> 70%)的 2.8 倍。
01
NK细胞背后的“功能暂歇”真相
一项发表在《Cell》的716名患者、24种癌症的大规模研究揭示了一个令人震惊的事实:NK细胞在对抗癌症的过程中,其功能状态会随肿瘤微环境发生变化。

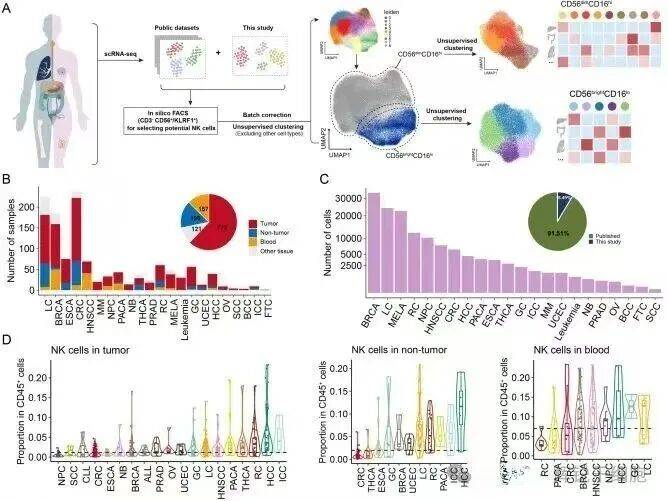
在这项大规模研究中,科学家们整合了716名患者、24种癌症类型的单细胞数据,仔细分析了超过16万个NK细胞。尽管NK细胞天生强大,但在复杂的肿瘤环境中,它们可能进入一种功能抑制状态,这种状态与肿瘤的进展和转移存在显著关联。
他们发现,不同癌症中的NK细胞状态差异明显:有些癌症如鼻咽癌、皮肤基底细胞癌中的NK细胞多为“未成熟型”,就像经验不足的“新兵”;而肾癌、肺癌中的NK细胞则以“成熟型”为主,看似战斗力更强。
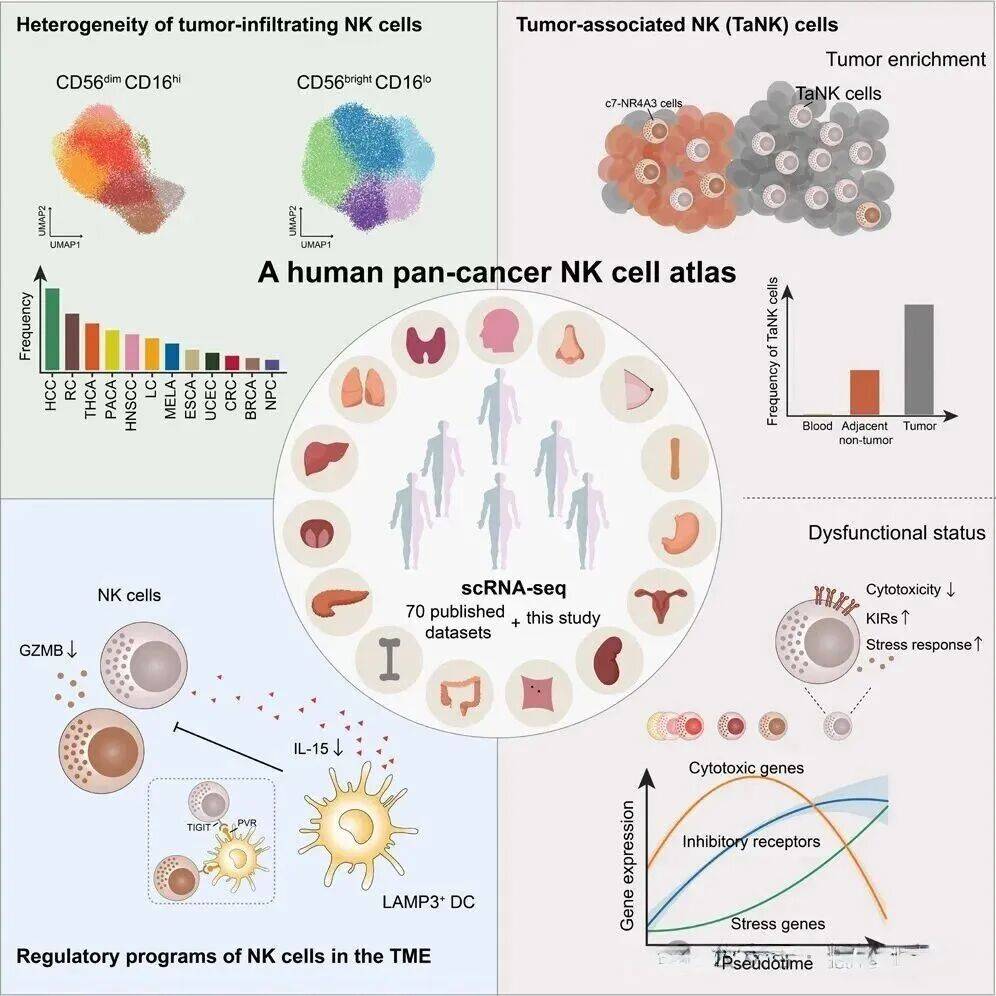
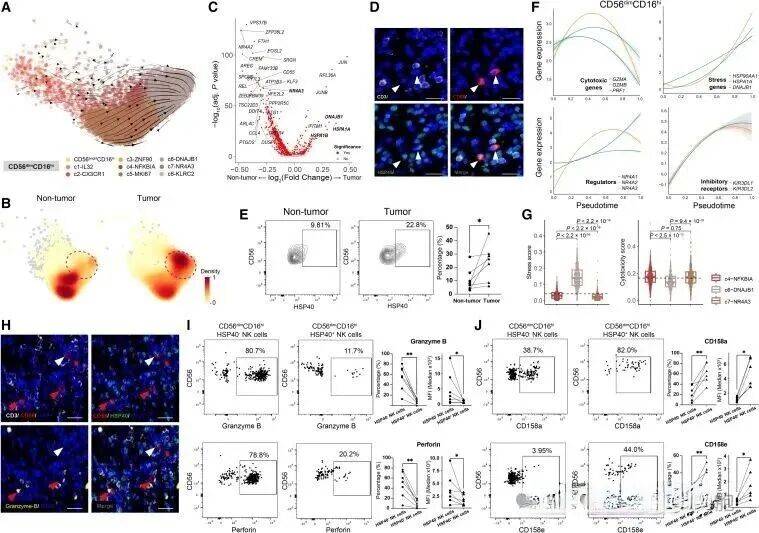
但最令人惊讶的是发现一种特殊的“肿瘤相关NK细胞”(TaNK)。这类细胞在肿瘤中数量增多,却更多处于“待机状态”——它们的杀伤武器(如GZMB、PRF1)减少,抑制性受体(TIGIT)却增多,整体作战能力大幅下降。
这些NK细胞处于潜在功能失调状态,虽然存在于肿瘤中,却已经失去了有效的杀伤能力。这种状态类似于T细胞的“耗竭”,但有着独特的分子特征。
这一现象的背后,并非 NK 细胞主动 “退缩”,而是肿瘤微环境对其产生的过度抑制,使其暂时难以启动杀伤程序。
03
功能暂歇的NK细胞为何影响免疫治疗效果?
免疫检查点抑制剂(ICB)等免疫疗法改变了癌症治疗格局,但令人沮丧的是,整体有效率仍不足30%。当NK细胞活性降低时,这些治疗手段的效果大打折扣。
《Cell》研究显示,NK细胞的高丰度与多种癌症的不良预后和免疫治疗耐药相关。这意味着,即使使用最新的免疫治疗手段,如果NK细胞功能不全,治疗效果仍然有限。
研究发现,特定的髓系细胞亚群,尤其是LAMP3+树突状细胞,似乎介导了NK细胞抗肿瘤免疫的调节。这些细胞通过某种机制抑制了NK细胞的活性,使得肿瘤能够逃避免疫监视。
04
免疫细胞:为人体补充健康的免疫力量
面对NK细胞在癌症中的“功能暂歇”,如何为人体补充 “健康的免疫力量”,成为近年来医学研究与健康管理的热点, 免疫细胞技术,,为未来可能的癌症治疗或免疫功能衰退提供 “细胞资源”。
免疫细胞的活性会随年龄增长、生活习惯(如熬夜、酗酒)、疾病状态而逐渐下降 ——研究发现,19-44岁人群NK细胞活性每降10%,癌症风险飙升27%;45岁后,NK细胞数量每年减少1.5%,免疫力随之大幅下降;65岁老人体内NK细胞战斗力仅为年轻人的三分之一。

NK 细胞作为人体抗癌的 “天生战士”,其活性与功能直接决定了免疫系统的抗癌能力。《Cell》研究揭示的 NK 细胞 “功能暂歇” 现象,不仅让我们更深入理解癌症进展的机制,也为免疫治疗的优化提供了新靶点。
而免疫细胞技术,通过补充NK 细胞,既可为癌症治疗提供 “细胞武器”,也为健康人群的免疫防护提供了新选择。