编者按:HER2阳性胃癌是一种恶性程度高、预后差的消化道肿瘤。尽管HER2靶向治疗改善了患者结局,但耐药性仍是严峻挑战。抗体偶联药物(ADC)如德曲妥珠单抗(Trastuzumab Deruxtecan,T-DXd)的出现,为HER2靶向治疗耐药患者带来了新希望。一项发表于Gastric Cancer的研究深入探讨了可逆与不可逆HER2酪氨酸激酶抑制剂(TKI)在调控HER2蛋白表达、下游信号及与T-DXd协同作用中的分子机制。研究发现,不可逆HER2-TKI吡咯替尼(Pyrotinib)通过促进HER2与分子伴侣HSP90解离,诱导HER2泛素化及蛋白酶体降解,并显著增强HER2内化和T-DXd的细胞内摄取,从而在体外和体内模型中均显示出强大的协同抗肿瘤效应。这为优化HER2阳性胃癌的联合治疗策略提供了重要的理论依据。
01
研究方法
研究者通过蛋白质印迹法评估HER2-TKIs对HER2及下游信号通路的影响;采用蛋白酶体抑制剂处理和免疫共沉淀实验,探究蛋白酶体降解在HER2表达调控中的作用;利用免疫荧光实验阐明HER2内化机制。通过HER2阳性胃癌细胞培养中的生长和活力实验,以及小鼠异种移植模型中的肿瘤生长和免疫组织化学染色实验,验证不可逆HER2-TKI吡咯替尼与T-DXd联合使用的协同潜力。
02
研究结果
可逆与不可逆HER2-TKI对HER2水平的影响相反
NCI-N87和SNU216细胞均过表达HER2蛋白,且NCI-N87细胞的HER2表达水平显著高于SNU216细胞。两种细胞经不同浓度和作用时间的可逆HER2-TKI(拉帕替尼、图卡替尼)和不可逆HER2-TKI(吡咯替尼、波齐替尼)处理后,均以浓度和时间依赖性方式抑制p-HER2水平,并降低下游效应分子p-AKT和p-ERK的表达,表明这些药物均能有效抑制HER2激酶活性。但两类药物对HER2总蛋白表达水平的影响存在显著差异:可逆HER2-TKI拉帕替尼和图卡替尼以浓度和时间依赖性方式增加HER2蛋白表达水平,而不可逆HER2-TKI吡咯替尼和波齐替尼则降低HER2蛋白表达,提示二者在HER2阳性胃癌中的作用机制存在本质区别(图1)。
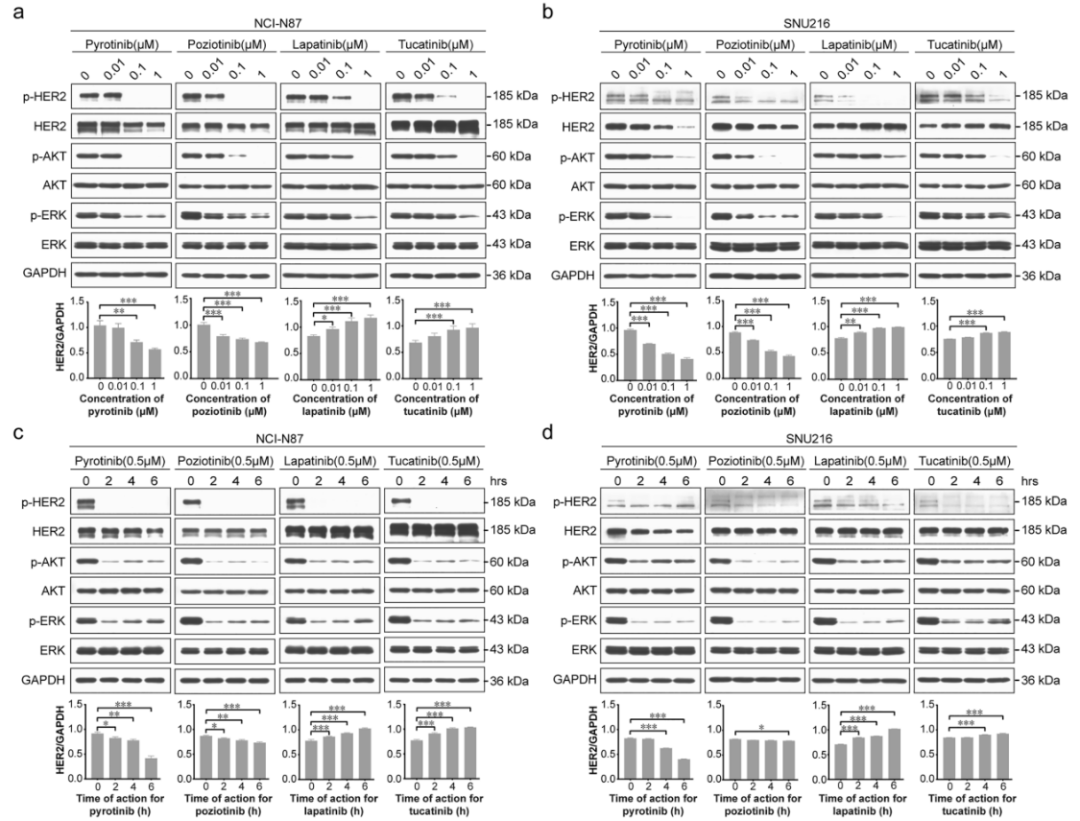
图1. 不同HER2-TKIs对HER2阳性胃癌细胞中HER2表达及下游信号通路的调控作用
不可逆HER2-TKI吡咯替尼通过促进HER2与HSP90解离增强HER2降解
qRT-PCR结果显示,拉帕替尼和吡咯替尼处理后,HER2 mRNA水平均呈时间依赖性增加,表明拉帕替尼诱导的HER2上调可能通过转录水平介导,而吡咯替尼诱导的HER2下调可能涉及转录后调控机制。为探究吡咯替尼降低HER2蛋白水平的机制,在吡咯替尼处理前30分钟,向细胞中加入蛋白酶体抑制剂MG132、Velcade或溶酶体抑制剂Bafilomycin A1(Baf-A1)。结果显示,MG132和Velcade可促进HER2蛋白水平升高,而Baf-A1对吡咯替尼诱导的HER2降解无影响,提示吡咯替尼通过泛素-蛋白酶体途径诱导HER2下调(图2)。
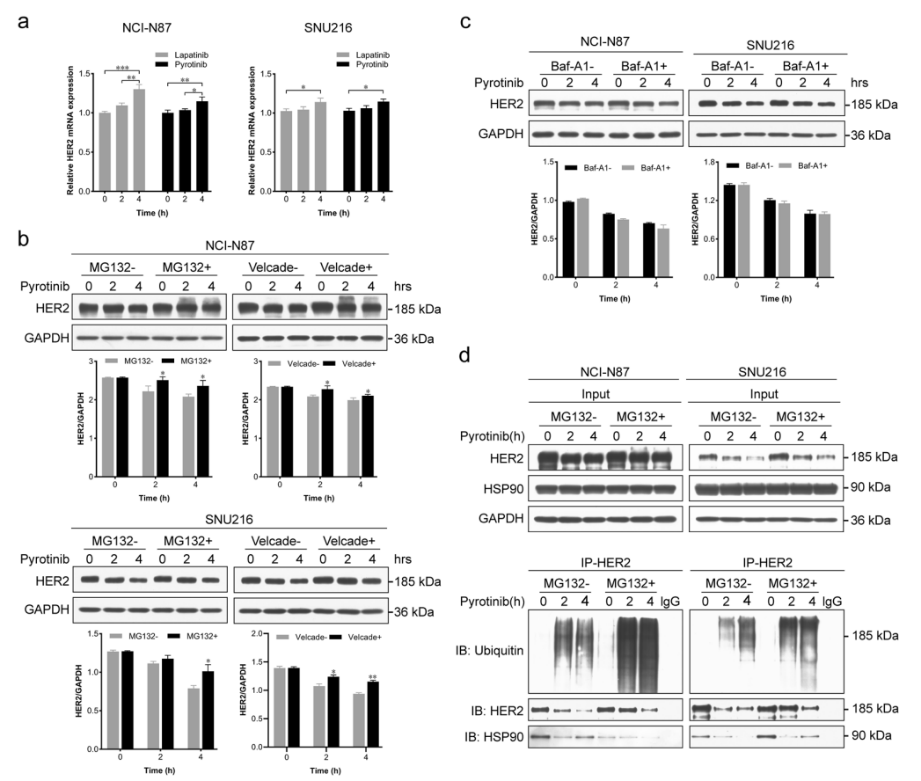
图2. 吡咯替尼通过诱导HSP90与HER2解离,增强HER2泛素化及后续的蛋白酶体降解
分子伴侣HSP90可保护HER2等客户蛋白免受泛素介导的降解。免疫共沉淀实验表明,吡咯替尼处理后,HER2泛素化水平显著增强,且与HER2共免疫沉淀的HSP90量明显减少(图2),说明吡咯替尼可减弱HER2与HSP90的相互作用。相反,拉帕替尼则降低HER2泛素化水平,这可能是可逆与不可逆HER2-TKI作用差异的关键原因。进一步研究发现,HER2的细胞内酪氨酸激酶结构域与HSP90存在相互作用,不可逆HER2抑制剂可能通过竞争性靶向该结构域,阻碍HSP90与HER2的结合。
不可逆HER2-TKI吡咯替尼增强HER2内化并促进T-DXd内吞
免疫荧光实验显示,未处理的NCI-N87和SNU216细胞中,HER2主要定位于细胞膜;拉帕替尼处理后,细胞膜上的HER2积累增加;而吡咯替尼处理则显著减少HER2的膜分布,并伴随细胞内点状结构增多。对NCI-N87细胞进行不同时间的吡咯替尼处理后,免疫荧光染色显示,未处理细胞中HER2与HSP90主要在细胞膜上共定位,随着吡咯替尼处理时间延长,二者在细胞膜上的共定位荧光强度逐渐减弱,提示吡咯替尼可能通过诱导HSP90与HER2解离,促进HER2的亚细胞转运(图3)。
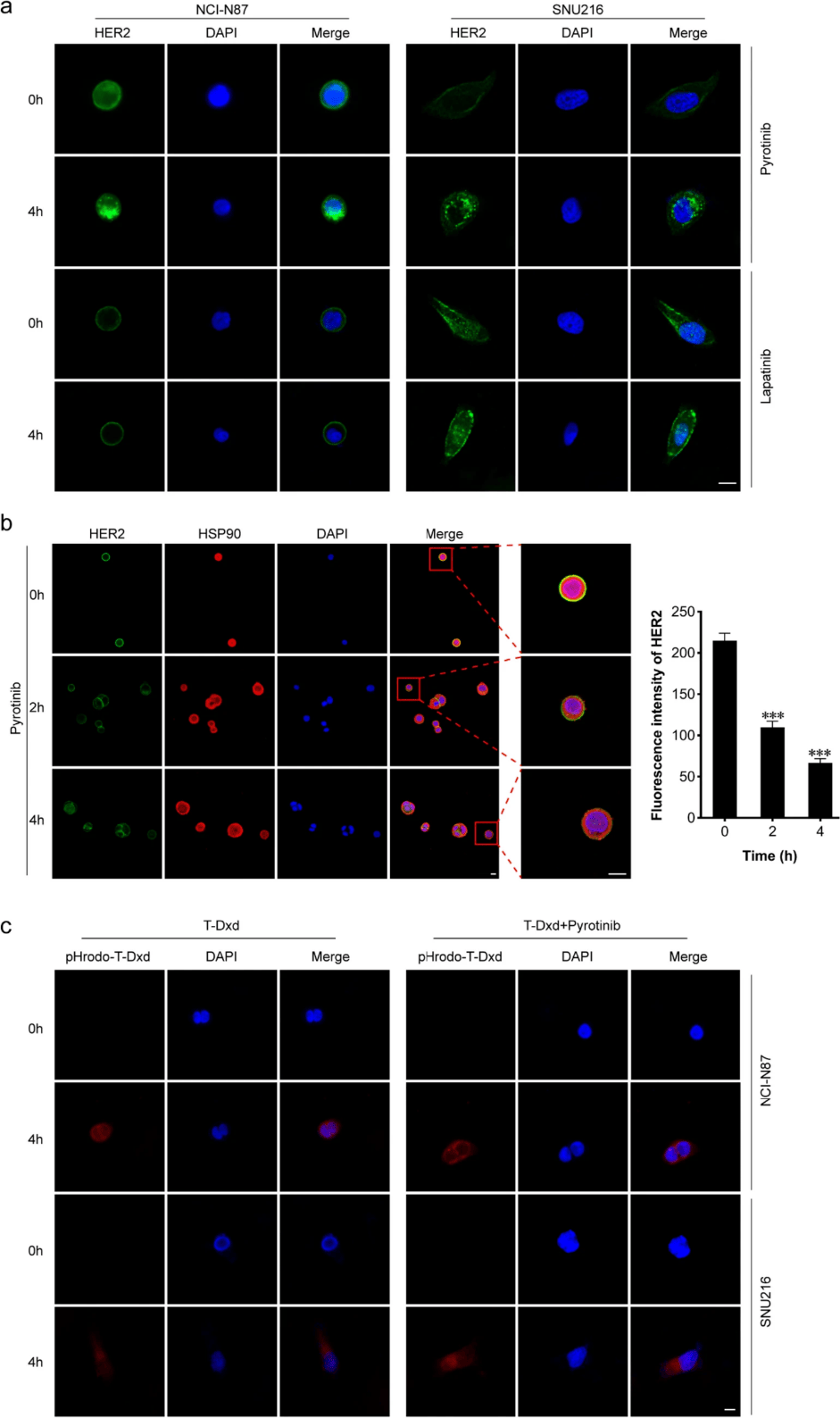
图3. 吡咯替尼增强HER2内化及T-DXd细胞内摄取
荧光标记T-DXd实验显示,NCI-N87和SNU216细胞在处理4小时后均能检测到红色荧光,表明T-DXd已被内吞;而吡咯替尼与T-DXd联合处理组的细胞内荧光信号更强,提示吡咯替尼可增强T-DXd的细胞内摄取(图3)。
吡咯替尼增强T-DXd对HER2阳性胃癌细胞的细胞毒性
在无T-DXd存在的情况下,通过剂量-效应曲线确定了对细胞生长影响轻微的吡咯替尼和拉帕替尼剂量(NCI-N87细胞中为0.01μM,SNU216细胞中为0.05μM)。将这些剂量的HER2-TKI与不同浓度的T-DXd联合使用后发现,拉帕替尼与T-DXd联合的生长抑制效果与T-DXd单药无显著差异,而吡咯替尼与T-DXd联合则显示出比T-DXd单药更强的生长抑制作用,表明非毒性剂量的吡咯替尼可协同增强T-DXd的细胞毒性。
吡咯替尼在NCI-N87异种移植小鼠模型中协同增强T-DXd的肿瘤抑制作用
体内实验中,吡咯替尼或T-DXd单药治疗对肿瘤生长的抑制作用有限,而二者联合治疗则展现出更强的抗肿瘤效果,显著优于单药治疗。且联合治疗组小鼠的体重与单药治疗组相比无显著变化,表明在增强抗肿瘤疗效的同时未增加额外毒性。
肿瘤组织的IHC染色显示,所有组均出现强HER2膜染色(评分3+),但吡咯替尼和T-DXd单药组的HER2染色较对照组减弱,联合治疗组的减弱更为明显。Western blot分析进一步证实,与对照组相比,单药组的HER2蛋白表达降低,而联合治疗组的HER2蛋白表达降低更为显著,表明吡咯替尼和T-DXd可独立降低HER2蛋白表达,联合使用时则协同增强HER2降解。
03
结论
本研究证实,不可逆HER2-TKI处理可显著降低HER2阳性胃癌细胞中的HER2蛋白水平,这一过程主要通过促进HSP90与HER2解离,增强HER2泛素化及蛋白酶体降解实现。同时,不可逆HER2-TKI吡咯替尼可有效促进HER2内化,显著增强ADC药物T-DXd的内吞作用,在体外和体内模型中均展现出协同抗肿瘤效果。这种联合治疗策略通过机制互补提升治疗效果,有望降低给药剂量并减少不良反应,为HER2阳性胃癌患者提供更有效的治疗选择。未来需开展进一步的临床研究,验证这一联合方案的临床价值,推动其转化为优化的治疗方案。
本资料仅供医疗卫生专业人士参考,请勿向非医疗卫生专业人士发放